CarbonBack – Prädiktion humantoxikologischer Wirkung synthetischer Carbon Black Nanopartikel
Das Verbundvorhaben hatte zum Ziel, valide Kriterien zur Abschätzung der toxischen Wirkungen von Carbon Black Nanopartikeln (CBNP) bei Exposition der Lunge bzw. der die Grenzfläche zwischen Umwelt und Organismus bildenden Lungenepithelien zu erarbeiten. Dabei sollte insbesondere untersucht werden, inwieweit das Gefährdungspotenzial mit definierten Materialeigenschaften korreliert.
Bisher ist unklar, ob das Gefährdungspotential in erster Linie durch die Partikelgröße und –geometrie oder durch die Oberflächenchemie determiniert wird.
Die Verbundpartner haben daher im Rahmen von 5 Teilprojekten die toxischen Effekte von CarbonBlack Nanopartikeln (CBNP) analysiert. Dabei wurden nicht-modifizierte CBNP solchen, die mit polyaromatischen Kohlenwasserstoffen (PAK) gecoatet wurden, gegenübergestellt. Neben Printex®90 als nicht modifizierten Referenzpartikel wurden auf Basis von Printex®90 hergestellte CBNP erzeugt und verwendet, die mit Benzo[a]pyren oder 9-Nitroanthracen gecoatet wurden, sowie Acetylenruß, der eine Mischung verschiedener PAK auf der Oberfläche trug. Basis für alle Analysen der biologischen Effekte stellten chemisch und physikalisch eingehend charakterisierte CBNP dar, die standardisiert suspendiert und anschließend an die Teilprojekte zur Testung in Modellsystemen steigender Komplexität verschickt wurden.
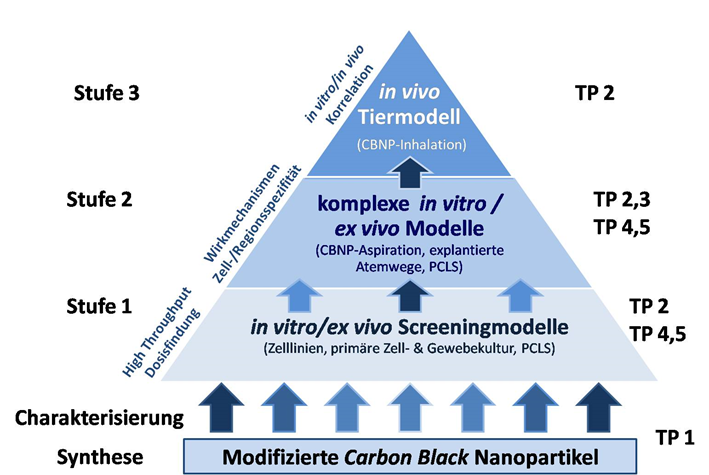
Dies erlaubte es, die Ergebnisse, die in den einzelnen Teilprojekten gewonnen wurden, untereinander vergleichen und eine abschließende Gesamtbewertung der Befunde aus allen Teilprojekten vornehmen zu können. Durch Implementierung einer Inhalationsstudie nach OECD 412 war ein Abgleich der Ergebnisse aus den in vitro / ex vivo Testsystemen mit der invivo-Situation möglich.
In der Gesamtschau der Ergebnisse zeigte sich, dass die Wirkung der Partikel in den biologischen Systemen maßgeblich durch die chemische Natur ihrer Oberfläche bestimmt wird. Die stärksten biologischen Effekte zeigten sich in den in-vitro und ex-vivo Systemen bei Exposition mit Acetylenruß. Die Effekte gingen weitestgehend mit der durch die jeweiligen CBNP induzierten mRNA-Expression der Cytochrom-P450-Oxidoreduktasen CYP 1A1 und Cyp 1B1 einher, die mit einer gesteigerten Zelltoxizität insbesondere bei Zellen mit sekretori-scher Funktion verknüpft waren. Acetylenruß erwies sich als einziges CBNP, durch das die mRNA-Expression von pro-inflammatorischen Zytokinen/Chemokinen induziert wurden.
Die Stärke der Effekte auf das Atemwegsepithel der Maus nahm von der Trachea hin zu den Bronchiolen ab. Die Induktion pro-inflammatorischer Zytokine im Lungenparenchym ist bei Geweben von Ratte und Mensch stärker ausgeprägt als bei der Maus, wie vergleichende Experimente an Precision-Cut-Lung-Slices (PCLS) zeigten. Nach oropharyngealer Aspiration der CBNP-Suspensionen, führte Acetylenruß zu einer erhöhten Anzahl von aus der Lunge isolierbaren Alveolarepithelzellen Typ II und zur veränderten mRNA-Expression bei Schlüsselenzymen der alveolären Surfactantsynthese.
Die Befunde der in-vitro und ex-vivo Testsysteme stehen in Einklang mit der durchgeführten in-vivo Inhalationsstudie. Im Expositionsversuch von Ratten nach OECD-412 wurden keine nennenswerten toxischen Effekte festgestellt. Lediglich Acetylenruß führte zu einer sehr moderaten Entzündung.
Die Ergebnisse dieses Projekts legen nahe, dass die biologischen/toxischen Effekte von CBNP durch Funktionalisierung der CBNP-Oberfläche mit PAK gesteigert werden, sofern die exponierten Zellen durch Expression von Cytochrom-P450-Oxidoreduktasen sensibel auf PAK reagieren können. Zellkulturmodelle, die diese Eigenschaft nicht besitzen, werden diese Effekte nicht detektieren können. Die Ergebnisse legen auch nahe, dass die akute pulmonale Toxizität von nicht modifizierten CBNP wie PAK-gecoateten CBNP gering ist.
Teilprojekte
TP 1: Spezifisch modifizierte Carbon Black Nanopartikel (CBNP) durch Gasphasensynthese (Karlsruher Institut für Technologie)
TP 2: Tox-Screening in vitro – Inhalation in vivo (Fraunhofer Institut für Toxikologie und Experimentelle Medizin)
TP 3: Wirkung von Carbon Black Nanopartikeln auf das Trachealepithel (Universität Lübeck)
TP 4: Atemwegregionsspezifische Wirkungen von Carbon Black Nanopartikel (Forschungszentrum Borstel)
TP 5: Toxikologische Wirkungen von CBNP auf Typ II Pneumozyten und Clara Zellen (Philipps-Universität Marburg)