Der Begriff Blut-Luft-Schranke beschreibt eine dünne zelluläre Trennschicht innerhalb der Lunge, die den luftgefüllten Raum der Lungenbläschen vom Blutkreislauf abgrenzt. Über diese Schranke wird die Aufnahme von Sauerstoff in das Blut und die Abgabe von Kohlenstoffdioxid in den Lungenraum geregelt. Mit der Atemluft können auch körperfremde Objekte abhängig von ihrer Größe in die Lunge gelangen. Dazu zählen neben Bakterien und Viren auch Feinstaub oder Nanomaterialien. Da die Zellschranke sehr dünn ist, besteht für Nanopartikel eine relativ große Chance, diese zu überwinden und in den Körper einzudringen.
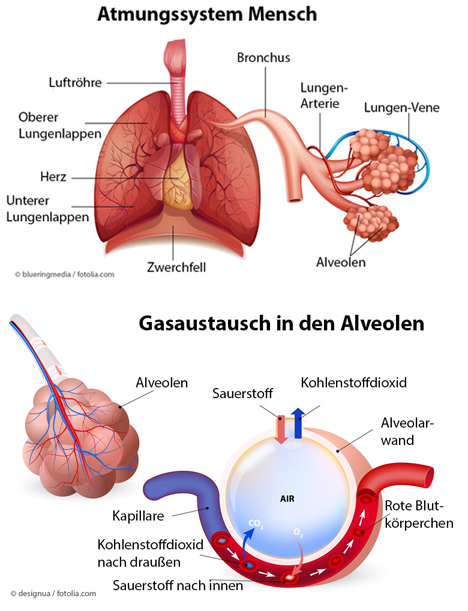
Die Lunge eines erwachsenen Menschen hat eine riesige Oberfläche (120m2 – 140m2), was der Fläche eines halben Tennisplatzes entspricht. Sie setzt sich aus einer Abfolge miteinander verbundener Luftwege zusammen. Dazu zählen die Luftröhre, gefolgt von den Bronchien, Bronchiolen bis hinunter zu den Lungenbläschen (Alveolen). Die Lungenbläschen ihrerseits, der Ort des Gasaustausches von Sauerstoff und Kohlenstoffdioxid, werden durch Epithelzellen geformt, die auf ihrer Innenseite direkten Kontakt mit den Endothelzellen der Blutgefässe haben. Diese alveolare Grenze trennt den Luftraum innerhalb der Lunge vom Blut in den Blutgefässen und kann mit bis zu 200 – 500 nm sehr dünn sein [1].
Da die Atemluft eine Reihe von Verunreinigungen wie Keime und Staubpartikel enthält, stehen der Lunge spezielle Reinigungsmechanismen zur Verfügung, um diese Verunreinigungen wieder zu entfernen. Normale Atemluft enthält zwischen 1.000 und 10.000 Mikroben/Keime sowie zwischen 10 und 50 Mikrogramm Fein- und Ultrafeinstaub pro Kubikmeter. Das bedeutet, dass ein Erwachsener mit 10.000 – 15.000 Litern Atemluft täglich mehr als 10.000 Mikroben und 10 Milliarden Partikel einatmet.
Zu den Reinigungsmechanismen des Körpers gehören zum einen die Fresszellen (alveolare Makrophagen) und zum anderen die sogenannte mukoziliäre Reinigung der oberen Atemwege durch Flimmerhärchen. In Abhängigkeit von ihrer Grösse lagern sich die Partikel in verschiedenen Regionen der Lunge ab, wobei Kleinstpartikel bis in die Lungenbläschen gelangen können. Hier werden die Partikel von den Fresszellen aufgenommen und über die Bronchiolen und Bronchien nach oben in Richtung Rachen transportiert. Grössere Partikel werden durch die mukoziliäre Reinigung, auch als mukoziliäre Rolltreppe bezeichnet, direkt nach oben in Richtung Rachen transportiert. Schlussendlich wird der Schleim mit den Fremdsubstanzen durch Schlucken, Abhusten oder Ausspucken aus der Lunge entfernt.
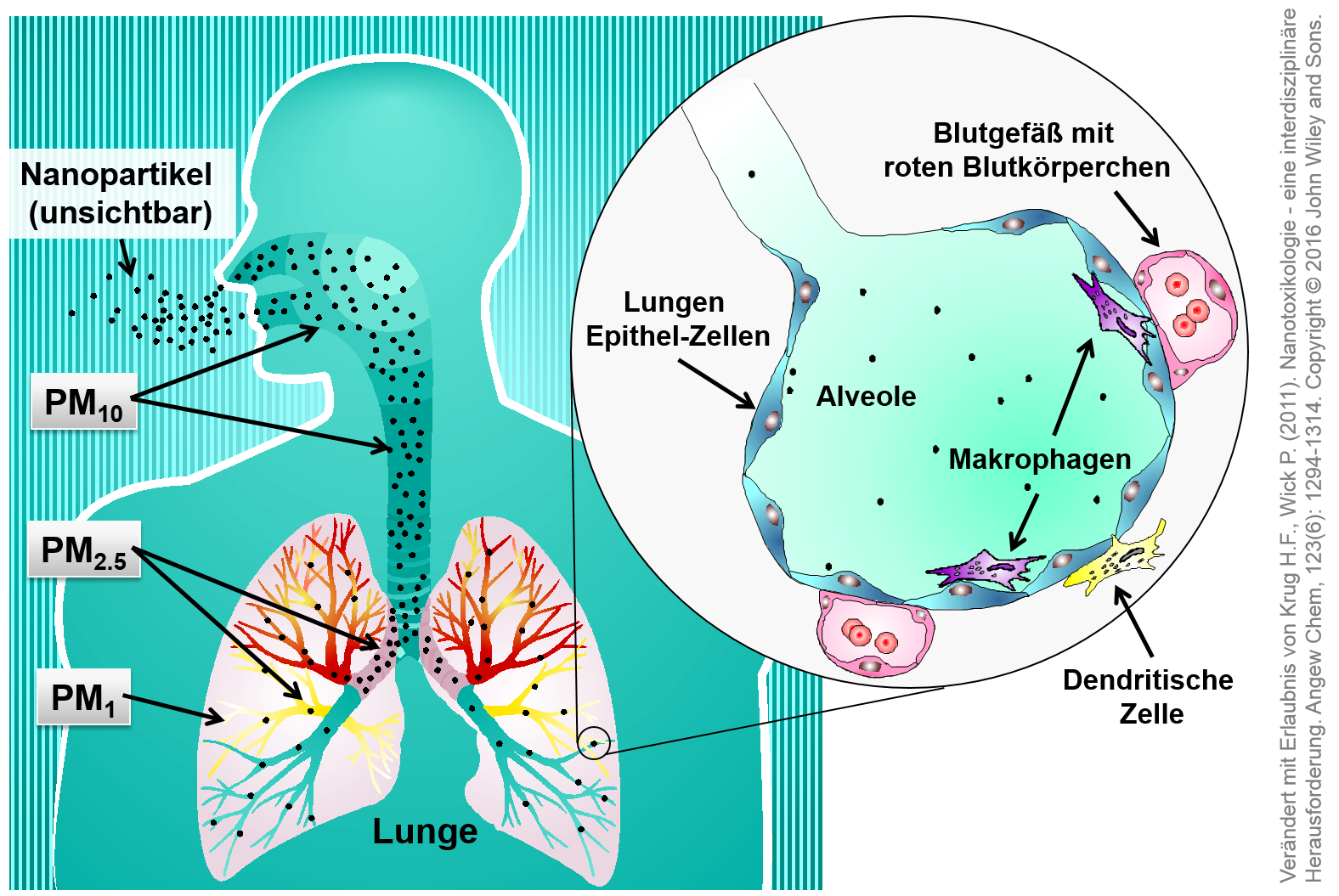
Die Grösse der Feinstaub-Partikel (engl. particulate matter, PM) beeinflusst nicht nur deren Ablagerung in den verschiedenen Bereichen der Atemwege sondern auch den möglichen Übertritt in den Blutstrom. Dabei unterscheidet die Feinstaub-Definition der Weltgesundheitsorganisation (WHO) zwischen inhalierbaren, Brustkorb- und alveolen-gängigen Stäuben. Nach dieser Definition gelangt die einatembare Staubfraktion in die oberen Atemwege wie Mund, Nase und Rachen (PM10 < 10 µm). Die Brustkorb-gängige Staubfraktion ist deutlich kleiner und erreicht die Bronchien und Bronchiolen (PM2.5 < 2.5 µm). Die alveolen-gängige Fraktion enthält die kleinsten Partikel (PM1 < 1 µm). Diese erreichen die Gasaustauschregion der Lungenbläschen und sind potentiell in der Lage, die Zellschranke zu überwinden und den Blutstrom zu erreichen [2,3,4].
Tatsächlich gibt es Hinweise, dass ein sehr kleiner Anteil der inhalierten Gesamtmenge (weniger als 1 Partikel pro Million) den Blutstrom erreicht und in sekundären Organen wie Nieren, Leber, Herz, Milz und anderen enden. Es wird diskutiert, dass Partikel zu Atemwegs-, Entzündungs- und Herzkreislauferkrankungen beitragen können [5,6]. Diese Effekte sind bekannt durch Staubbelastung an Arbeitsplätzen (wie z.B. im Bergbau) oder während schwerer Luftverschmutzungen wie den Smog Episoden 2015 in Peking (China) oder der dramatische Smog-Episode 1952 in London (UK). Im Falle gravierender Luftverschmutzung kann die Partikelmenge in der Luft auf bis zu 1.000 Mikrogramm Staubpartikel ansteigen, was mehreren Millionen Partikeln pro cm3 (1 Milliliter) entspricht.
Nanomaterialien fallen aufgrund ihrer Größe in die gleiche Kategorie wie die kleinste PM-Fraktion (PM1) und sollten daher theoretisch ebenfalls in der Lage sein, die Blut-Luft-Schranke zu überwinden. Der Großteil einer verabreichten Dosis wird jedoch von den Fresszellen erkannt und aus der Lunge heraus transportiert werden [3,4].
Heutzutage werden Nanomaterialien bereits in einer Vielzahl von Produkten z.B. bei der Oberflächenbeschichtung, in Farben, Textilien oder technischem Equipment verwendet. Daher ist das Einatmen dieser Nanomaterialien während der Herstellung aber auch während der Benutzung und Entsorgung möglich. Zudem gibt es einige Medizinprodukte mit Nanopartikeln, die zur Diagnose oder Therapie von Krankheiten eingesetzt werden, um entweder direkt die Lunge zu behandeln oder die Lunge als Verabreichungsweg zu nutzen (vgl. Querschnittsartikel Nanomedizin).
Es ist daher sehr wichtig, zwischen einer gewollten Exposition (medizinische Behandlung) und ungewolltem Einatmen z.B. am Arbeitsplatz zu unterscheiden. Erwiesenermaßen ist die Lunge der kritischste Eintrittsweg für Nanomaterialen in den Körper. Deshalb gibt es spezifische Regulierungen und Schutzmassnahmen für Arbeitsplätze mit hoher Staubbelastung. In Deutschland ist dafür die Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA) zuständig [7,8].
Verschiedenste Studien haben gezeigt, dass das Einatmen von Metalloxiden und anderen Nanopartikeln in hoher Konzentration zu Lungenentzündungen führen kann, wenn diese in die Kategorie der sogenannten granulären biobeständigen Stäube (GBS) fallen [9,10]. Darüber hinaus ist aber auch die geometrische Struktur eines Nanomaterials entscheidend für dessen Lungentoxizität. Es wurde befürchtet, dass die strukturellen Ähnlichkeiten von Mineralfasern und technisch hergestellten Nanofasern einschliesslich Nanoröhrchen, Nanostäben und Nanodrähten dazu führen könnten, dass sich diese unter bestimmten Umständen wie Asbest Fasern verhalten könnten. Nachweislich verursachen aber nicht alle Nanofasern, sondern nur lange und dünne Nanofasern ähnlich wie lange Asbest Fasern Langzeitentzündungen und starke Fibrose im Lungengewebe [5,11,12].
In Deutschland werden diese Wechselwirkungen in Projekten wie CaNTser, nanoCOLT und CarboTox untersucht, die vom Bundesministerium für Bildung und Forschung (BMBF) gefördert werden.
Viele epidemiologische Studien haben gezeigt, dass die Belastung der Lunge mit ultrafeinen Partikeln direkt mit einigen schweren Erkrankungen besonders nach Langzeitinhalation zusammenhängt. Daher ist es besonders wichtig, diese Effekte eingehend für technisch erzeugte Nanomaterialien zu untersuchen, um eine Belastung mit schädlichen Nanomaterialien zu verhindern.
Literatur
- Gehr, P et al. (2006), Paediatr Respir Rev, 7 Suppl 1S73-S75.
- Krug, HF et al. (2011), Angew Chem Int Ed, 50(6): 1260-1278.
- Kreyling, WG et al. (2013), Acc Chem Res, 46(3): 714-722.
- Kreyling, WG et al. (2013), ACS Nano, 8(1): 222-233.
- Braakhuis, HM et al. (2014), Part. Fibre Toxicol, 11: 18.
- Saber, AT et al. (2014), WIREs Nanomed Nanobiotechnol 2014, 6: 517–531.
- Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA) – Nanotechnologie
- IUTA/BAuA/BG RCI/IFA/TUD/VCI (2011). Tiered Approach to an Exposure Measurement and Assessment of Nanoscale Aerosols Released from Engineered Nanomaterials in Workplace Operations (PDF, 2 MB) .
- Donaldson, K et al. (2012), Acc Chem Res, 46(3): 723-732.
- Ausschuss für Gefahrstoffe – AGS-Geschäftsführung – BAuA (2015). Beurteilungsmaßstab NanoGBS – Beurteilungsmaßstab für technisch gezielt hergestellte ultrafeine Stäube aus alveolen-gängigen granulären biobeständigen Stäuben ohne bekannte signifikante spezifische Toxizität (nanoskalige GBS) (A-Staub), Fassung 3.32015, Juni 2015. (PDF, 182 KB)
- Donaldson, K et al. (2013), Adv Drug Deliv Rev, 65(15): 2078-2086.
- Schinwald, A et al. (2012), Toxicol Sci, 128(2): 461-470.